蔡正维医生的科普号
- 精选 男孩变声后还能长多高?知道真相后惊呆了!
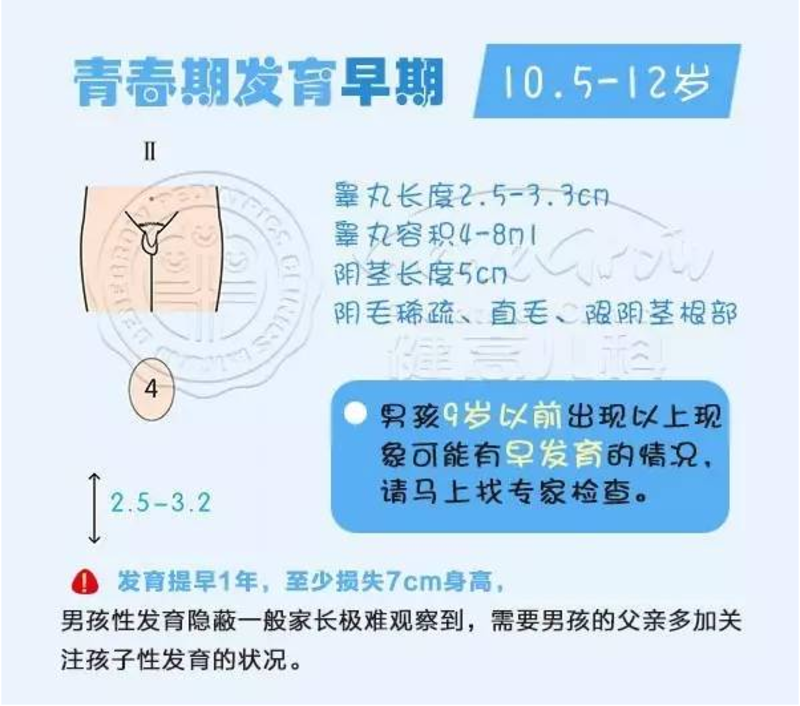
健高成长之家 今天 青春发育期会带来身高和体重的快速增长,但如果要问男孩什么时候进入青春发育期、标志是什么,可能很多家长会说变声、长胡须、喉结或者初次遗精等。 事实上,这些都不是男孩青春期开始的标志。 「 男孩的发育顺序 」 正常情况下,男孩10.5岁左右进入青春发育期,以睾丸的发育为标志,发育顺序为: 10~11岁,睾丸开始发育; 11~12岁,阴囊发育和色素沉着,阴茎发育; 12~13岁,肾上腺功能出现 ,阴毛发育; 13~14岁,睾丸和阴茎迅速发育,乳腺组织发育; 14~15岁,腋毛、痤疮、声音变调,初次遗精。 「 相关文献报道 」 由于男孩青春期开始发育的标志比较隐蔽,如果孩子不说,家长一般难以察觉到。等到孩子出现变声、痤疮、长胡须或者喉结等外在特征比较明显的情况时,孩子往往已经进入了青春期的中后期。 此时,身高突增高峰期已过,身高的增长空间已经很少。 据报道: 男孩青春期身高突增高峰基本位于男生变声前,此时由于生长激素分泌增加,促进骨骼的生长,每年长高不少于6-8cm。 在变声后,身高增长明显放缓,直至停止增长,这是由于青春期之后性激素分泌增加使骨骺板成熟停止发育导致身高固定。 临床医学表明: 一般情况下,人的骨骺在14、15岁(初中二三年级)时候就会闭合,一旦骨骺闭合,无论任何方法,都不可能再长高。 当男孩出现变声时,表明身高开始进入停长倒计时,身高至多再长5-7.5cm,有些孩子甚至只能增长1-2cm。 如果男孩子变声时身高不高、不理想,家长还认为有足够的时间长个子,没有及时的进行干预,等到认识到有问题时,实际上已经错过了身高最后的干预机会!只要男孩变声时身高不足1米6,可能永远长不到1米7。 在现实生活中,还有很多的家长因为缺乏青春期生长发育知识,对孩子发育情况关注较少,当孩子在9岁前出现睾丸发育的情况时,并未发现,导致孩子出现早发育的情况。等到孩子比别人家的孩子提前出现胡须、变声时,才想到是否早发育,这时再去需求帮助往往己经晚了,错过了最佳的干预时机。 研究发现: 未经治疗的早发育儿童最终身高可能为155cm至160cm。 此外,早发育男孩由于身体发育很快,更向往模仿社会上的一些东西,如性爱和暴力,他们也因此比一般孩子更容易发生“危险”,产生犯罪和自杀等社会问题。 家长应多加关注孩子的发育状况,一旦发现早发育的的现象,尽快到专业的生长发育机构进行检查,及时干预是可以帮助孩子抓住自然长高时间的!
 蔡正维 主任医师 宜昌市中心人民医院 儿科1.4万人已读
蔡正维 主任医师 宜昌市中心人民医院 儿科1.4万人已读 - 精选 矮身材儿童诊治指南
【矮身材的定义】矮身材是指在相似生活环境下,同种族、同性别和年龄的个体身高低于正常人群平均身高2个标准差者(-2SD),或低于第3百分位数(-1.88SD)者,其中部分属正常生理变异,为正确诊断,对生长滞后的小儿必须进行相应的临床观察和实验室检查。【病因】导致矮身材的因素甚多,其中不乏交互作用者,亦有不少疾病导致矮身材的机理迄今未阐清(见表1)【诊断】对矮身材儿童必须进行全面检查,明确原因,以利治疗。 一、病史应仔细询问:患儿母亲的妊娠情况;患儿出生史;出生身长和体重;生长发育史;父母亲的青春发育和家庭中矮身材情况等。 二、体格检查除常规体格检查外,应正确测量和记录以下各项:①当前身高和体重的测定值和百分位数;②身高年增长速率(至少观察3个月以上);③根据其父母身高测算的靶身高;④BMI值;⑤性发育分期。 三、实验室检查 1.常规检查 应常规进行血、尿检查和肝、肾功能检测;疑诊肾小管中毒者宜作血气及电解质分析;女孩均需进行核型分析;为排除亚临床甲状腺功能低下,应常规检测甲状腺激素水平。2.骨龄(Bone Age,BA)判定 骨骼的发育贯穿整个生长发育过程,是评估生物体发育情况的良好指标,骨龄即是各年龄时的骨成熟度,是对左手腕、掌、指骨正位X线片观察其各个骨化中心的生长发育情况进行测定的。目前国内外使用最多的方法是G-P法(Greulich & Pyle)和TW3法(Tanner-Whitehouse),我国临床上多数采用G-P法。正常情况下,骨龄与实际年龄的差别应在±1岁之间,落后或超前过多即为异常。3.特殊检查(1)进行特殊检查的指征 ①身高低于正常参考值减2SD(或低于第3百分位数)者;②骨龄低于实际年龄2岁以上者;③身高增长率在第25百分位数(按骨龄计)以下者,即:<2岁儿童为<7CM/rh;④临床有内分泌紊乱症状或畸形综合征表现者;⑤其他原因需进行垂体功能检查者。(2)生长激素-胰岛素样生长因子-1轴(GH-IGF-1)功能测定 以往曾应用的运动、睡眠等生理性筛查试验目前已很少应用,多数都直接采用药物刺激试验(见表2)。(3)胰岛素样生长因子-1(IGF-1)和胰岛素样生长因子结合蛋白-3(IGFBP-3)测定 两者的血清浓度随年龄增长和发育进程而增高,且与营养等因素相关,各实验室应建立自己的参比数据。(4)IGF-1生成试验 对疑为GH抵抗(Laron综合征)的患儿,可用本试验检测GH受体功能。①方法一:按0.075-0.15U/(kg·d)每晚皮下注射rhGH 1周,于注射前、注射后第5和第8天各采血样一次,测定IGF-1;②方法二:按0.3 U/(kg·d)每晚皮下rhGH,共4d,于注射前和末次注射后各采血样1次,测定IGF-1,正常者的血清IGF-1在注射后会较其基值增高3倍以上,或达到与其年龄相当的正常值。(5)其他内分泌激素的检测 依据患儿的临床表现,可视需要对患儿的其他激素选择进行检测(6)下丘脑、垂体的影像学检查 矮身材儿童均应进行颅部的MRI检查,以排除先天发育异常或肿瘤的可能性。(7)核型分析 对疑有染色体畸变的患儿都应进行核型分析。【鉴别诊断】 根据病史,体检等资料分析,对营养不良、精神心理性家庭性特发性矮身材、小于胎龄儿、慢性系统性疾病等因素造成的非生长激素缺乏的矮身材比较容易识别 对常见的导致矮身材的病因应予以鉴别,如:软骨发育不良、甲状腺功能低下症、体质性青春发育延迟;临床还需注意某些综合征的可能,如:Prader-Willi综合征,Silver-Russeli综合征,Noonan综合征等。【治疗】1.矮身材儿童的治疗措施取决于其病因 精神心理性、肾小管酸中毒等患儿在相关因素被消除后,其身高增长率即见增高,日常营养和睡眠的保障与正常的生长发育关系密切。2.生长激素 随着基因重组人生长激素(rhGH临床应用经验的大量累积,目前获准采用rhGH治疗的病种逐渐增多,自1985年美国FDA批准rhGH治疗生长激素缺乏症以来,陆续核准的病病有慢性肾功能衰竭(1993)、先天性卵巢发育不全(1996-1997)、Prader-Willi综合征(2000)、小于胎龄儿(2001)和特发性矮身材(2003)。由于大部分小于胎龄儿在生后2-3年内都会呈现追赶生长,身高可以达到与其靶身高相称的生长曲线范畴,故对小于胎龄儿都应定期随访观察。一般在3周岁时,如其生长仍然滞后,应考虑GH治疗。2003年FDA批准GH用于特发性矮身材,即:①非GH缺乏的原因不明者;②身高低于同性别、同年龄儿正常参比值2.25SD以上;③预计其成人期终身高在-2SDS以下。(1)剂型 国内可供选择的有rhGH粉剂和水剂两种,后者的增长效应稍好。(2)剂量 生长激素的剂量范围较大,应根据需要和观察到的疗效进行个体化调整。目前国内常用剂量是0.1-0.15IU/kg·d,每周0.23-0.35mg/kg;对青春发育期患儿、Turner患儿、小于胎龄儿、特发性矮身材和某些部份性生长激素缺乏症患儿的应用剂量为0.15-0.20IU/(㎏.d)每周0.35-0.46(㎎.㎏)(注:WHO标注生长激素1㎎=30U)(3)用法:每晚睡前皮下注射1次,常用注射部位为大腿中部1/2的外、前侧面,每次注射应更换注射点,避免短期内重复而引致皮下组织变性。(4)疗程:生长激素治疗矮身材的疗程视需要而定,通常不宜短于1-2年,过短时患儿的获益对其终身高的作用不大。(5)副作用:常见的副作用为:①甲状腺功能减低:常在开始注射2-3月后发生,可按需给予L-甲状腺素片纠正;②糖代谢改变:长期较大量使用生长激素可能使患儿发生胰岛素抵抗。空腹血糖和胰岛素水平上升,但很少超过正常高限,停用生长激素数月后即可恢复,在疗程中应注意监测,对有糖尿病家族史者和肥胖儿尤须注意;③特发性良性颅内压升高:生长激素可引起纳、水潴留,个别患者会出现特发性颅内压升高、外周水肿和血压升高,多发生于慢性肾功能衰竭、Turner综合症和GH缺乏症所致生长障碍患儿,可暂停GH治疗,并加用小剂量(如:氢氯噻嗪)降低颅内压;④抗体产生:由于制剂纯度的不断提高,目前抗体产生率已减少,水溶液制剂更少;⑤股骨头滑脱、坏死:因为骨骼在治疗后生长加速、肌力增强,运动增多时可能引起股骨头滑脱、无菌性坏死、致跛行,亦可出现膝关节、髋关节疼痛,呈外旋性病理状态,可暂时停用GH并补充维生素D和钙片治疗⑥注射局部红肿或皮疹:通常在数日内消失,可继续使用,目前已甚少见⑦诱发肿瘤的可能性:国际上有关组织曾进行过相关调查研究,根据国家合作生长组和药物治疗研究中心等学术机构的大量流行病学资料,包括对肿瘤患者年龄、性别和种族等人群信息进行综合分析,结果显示无潜在肿瘤危险因素存在的儿童,GH治疗不增加白血病发生和肿瘤复发的危险,但对曾有肿瘤、有家族肿瘤发生遗传倾向、畸形综合征,长期超生理剂量GH应用时需谨慎,治疗过程中应密切监测血清IGF-1水平,超过正常参照值+2SD者宜暂时停用。3.其他药物:①疗程中应注意钙、微量元素等的补充,以供骨生长所需;②蛋白同化激素:常与生长激素并用治疗Turner综合征,国内大多使用司坦唑醇stanozolol,康力龙),常用剂量为0.025-0.05㎎/(㎏.d)需注意骨龄增长情况;③IGF-1性腺轴抑制(GnRHa),芳香酶抑制剂(Letrozole,来曲唑)等亦曾被用于治疗矮身材,国内目前无足够资料分析,故不建议常规应用。【随访】所有确诊矮身材患儿都应进行长期随访 使用生长激素治疗者每3个月应随访1次:测量身高(最好测算⊿SDS)此处还要进行IGF-1、IGFBP-3、T4、TSH、血糖和胰岛素等检测,以便及时调整GH剂量和补充甲状腺素。每年检查骨龄1次。疗程中应观察性发育情况,按需处理。疑有颅内病变者应注意定期重复颅部MRI扫描。(沈永年 王慕逖 整理)
蔡正维 主任医师 宜昌市中心人民医院 儿科2731人已读 - 精选 GnRHa治疗中枢性性早熟的新进展
蔡正维 谢宗兰 刘孝桥(三峡大学第一临床医学院 宜昌市中心人民医院 443003)中枢性性早熟(central precocious puberty)是由于儿童下丘脑-垂体-性腺轴功能提前启动,造成血清中促性腺激素和类固醇性激素浓度的提前升高达到青春期水平。随着近年来发病率明显增加,性早熟已成为儿童常见的内分泌疾病,性早熟问题也逐步引起人们的重视,性早熟可明显影响儿童的正常生长发育和社会心里健康。患儿的青春期高峰生长速度提前呈现,骨龄提前,骨骺提前闭合,最终导致成年矮身材、身体比例不协调,增加成年后内分泌相关疾病,如代谢综合征等的发病风险,同时还会产生相应的心理问题和社会问题 [1],因此延缓青春期发育及早干预治疗显得尤为重要。促性腺激素释放激素类似物(Gonadotropin-releasing hormone ,GnRHa)是国内外公认中枢性性早熟的标准治疗方案[2, 3]。GnRHa可保持内源性的GnRH释放的脉冲和幅度不变,同时其半衰期延长,持续作用于受体,使受体发生下降调节,对下丘脑-垂体-性腺轴( hypothalamus pituitary gonad axis,HPGA)产生高度抑制作用,抑制促性腺激素(LH、 FSH)分泌, 性腺发育停止,性激素下降甚至恢复至青春期水平[4] 。本文主要从促性腺激素释放激素类似物在中枢性性早熟治疗相关研究进展进行阐述。一、GnRHa治疗的指证我国目前规定女孩在8岁、男孩在9岁前呈现第二性征发育征象即为性早熟[2],在欧洲,青春期启动和女孩的初潮年龄在过去的50年里一直在提前,尤其在美国,男女青春期启动的平均年龄更早,目前许多儿科内分泌专家推荐对8岁前出现青春期的女孩,特别是那些青春期和骨龄进展快速者及预测成年期身高受损的女孩,进行谨慎细致的评估,这就要求临床上在判断性早熟时,应依据不同国家、不同种族的最新的标准进行评估[5]。因此并非所有性早熟患儿均需GnRHa的医学干预,对线性生长、骨骼成熟和第二性征发展加速以及预测成年升高低于正常均值减2SD的生长潜能明显受损但尚有剩余的中枢性性早熟患儿则应进行必要的治疗[2]。二、疗效及不良反应的监测及随访青春期是快速生长和骨骼生长、骨量达到顶峰的关键时期,使用GnRH类似物抑制下丘脑-垂体-性腺轴功能,青春期表现受到抑制甚至回缩,而影响患儿的骨骼增长。因此长期使用GnRHa的患儿至少每年要进行一次骨龄测定,定期检测性激素水平及性发育水平如:乳房分期、子宫、卵巢容积改变。治疗中可复查GnRH刺激试验,若刺激后LH峰值达到青春期前水平即指示抑制满意。GnRHa的副作用很小,大多是暂时性的,如局部反应、头痛、乏力、潮红等;部分女孩可出现首次注射后撤退性阴道出血;皮肤过敏反应很少见,但可以很严重。而人们更关注其药物长期的疗效及安全性,多项对GnRHa治疗的CPP女孩长期观察数据显示,应用GnRHa可帮助达到或接近遗传靶身高(通常在-2SD以内),且生殖系统不受到影响, 同时专家提出开始治疗时年龄越小,获得较预测身高增长越多[6]。但资料显示治疗前的体重指数(BMI)是预估治疗后发生超重和肥胖的最佳指标,肥胖的CPP患儿治疗后可能仍有体重的问题,在GnRHa治疗期间应该合理控制体重[7]。在对CPP的研究中观察到,骨密度在治疗中低于正常青春期的患儿,建议对使用GnRHa治疗的患者应补充钙剂。三、GnRHa联合GH治疗部分CPP患者应用GnRHa后出现生长速率过度下降,这种现象可视为一个阶段的“下降生长”,部分研究者认为其原因可能是由于GnRHa使生长激素在夜间的脉冲分泌峰降低,但其分泌峰频率仍正常[7];另外有人认为下丘脑-垂体-性腺轴的过度抑制对GH-IGF1轴有负性影响[3] ,如果生长状况不理想,应考虑加用生长激素。当应用GnRHa过程中出现明显生长减速,生长潜能受损尤其是已有初潮、骨龄超过11.5岁的患儿应联合应用生长激素,以改善成人身高,现认为应用GnRHa后,年增长速率≤4cm或预期成年身高无明显改善的患儿为联合GH的治疗时机[8, 9]。同时在对GnRHa的研究发现,生长激素缺乏症的青春期患儿,联合应用GnRHa3年可明显改善成人身高。有研究数据显示,过早进入青春期的特发性矮身材或者宫内发育迟缓的患儿,应用GH联合GnRHa治疗可提高成人身高7cm左右,但其临床应用尚待进一步商榷[10]。五、临床剂型的选择目前对于中枢性性早熟最佳的治疗方法是每隔4-12周使用一次GnRHa,这类GnRHa可持续数周、缓慢释放而抑制垂体分泌促性腺激素。在过去的二十年用药过程中,目前认为每3个月注射一次亮丙瑞林(11.25mg)也可以成功抑制青春期的发育;长效戈舍瑞林(10.8mg)治疗儿童中枢性性早熟亦有效,但其药效在使用后12周会减弱,因此建议每8周注射一次[11]。尽管对长期使用这些长效制剂的比较研究仍非常有限,但其抑制促性腺激素分泌改善最终成年期升高的疗效无明显差异。基于患者用药便利,避免频繁皮下注射的原则,目前皮下植入组氨瑞林(Histrelin)成为最新CPP患儿的治疗进展,通过皮下植入的微孔板可持续一年缓慢释放GnRHa,从而避免反复药物注射痛苦及剂量调整[12]。综上所述,中枢性性早熟患儿应首选GnRHa治疗,但需合理掌握应用指证,治疗中注意监测、评估生长及成熟的平衡,才能达到改善最终成年身高的目的。尽管在既往应用GnRHa有着良好的安全性和有效性,但是治疗过程中仍需严密监测,充分考虑社会、家庭等因素,制定个体化诊疗计划。1. Golub MS, Collman GW, Foster PM, Kimmel CA, Rajpert-De Meyts E, et al. Public health implications of altered puberty timing. Pediatrics 2008:121 Suppl 3:S218-230.2. 中华医学会儿科学分会内分泌遗传代谢学组 中枢性(真性)性早熟诊治指南. 中华儿科杂志 2007:45:2.3. Antoniazzi F, Zamboni G Central precocious puberty: current treatment options. Paediatr Drugs 2004:6:211-231.4. 郭红宇, 高云荷 GnRH类似物的研究进展. 中国实用妇科与产科杂志 2005:21:3.5. Kaplowitz PB, Oberfield SE Reexamination of the age limit for defining when puberty is precocious in girls in the United States: implications for evaluation and treatment. Drug and Therapeutics and Executive Committees of the Lawson Wilkins Pediatric Endocrine Society. Pediatrics 1999:104:936-941.6. Magiakou MA, Manousaki D, Papadaki M, Hadjidakis D, Levidou G, et al. The efficacy and safety of gonadotropin-releasing hormone analog treatment in childhood and adolescence: a single center, long-term follow-up study. J Clin Endocrinol Metab 2010:95:109-117.7. Heger S, Partsch CJ, Sippell WG Long-term outcome after depot gonadotropin-releasing hormone agonist treatment of central precocious puberty: final height, body proportions, body composition, bone mineral density, and reproductive function. J Clin Endocrinol Metab 1999:84:4583-4590.8. 李筠, 梁黎, 孙莉颖, 董关萍 联合应用促性腺激素类似物和生长激素治疗女性初潮后特发性中枢性性早熟. 中华儿科杂志 2005:43:2.9. Proos LA, Lonnerholm T, Jonsson B, Tuvemo T Can bone age determination provide criteria for growth hormone treatment in adopted girls with early puberty? Ups J Med Sci 2006:111:117-129.10. Wit JM, Balen HV, Kamp GA, Oostdijk W Benefit of postponing normal puberty for improving final height. Eur J Endocrinol 2004:151 Suppl 1:S41-45.11. Isaac H, Patel L, Meyer S, Hall CM, Cusick C, et al. Efficacy of a monthly compared to 3-monthly depot GnRH analogue (goserelin) in the treatment of children with central precocious puberty. Horm Res 2007:68:157-163.12. Eugster EA, Clarke W, Kletter GB, Lee PA, Neely EK, et al. Efficacy and safety of histrelin subdermal implant in children with central precocious puberty: a multicenter trial. J Clin Endocrinol Metab 2007:92:1697-1704.
蔡正维 主任医师 宜昌市中心人民医院 儿科9278人已读 - 精选 胰岛素和左旋多巴联合激发试验对儿童生长激素缺乏症的诊断价值
蔡正维刘孝桥熊安秀王敏张光环李红义高琴峰(三峡大学第一临床医学院湖北省宜昌市中心人民医院儿科,443003)【摘要】目的评价胰岛素和左旋多巴(L-dopa)联合激发试验对儿童生长激素缺乏症(GHD)的诊断价值。方法将219例生长发育迟缓儿童根据生长学资料、临床特征分为拟诊GHD组(119例)与非GHD组(100例),全部进行胰岛素+L-dopa联合激发试验、精氨酸激发试验(ARG)和可乐定激发试验,采用放射免疫分析分别测定激发试验前和激发试验后30min、60min、90min、120min的GH值,并分析两组实验的GH激发峰值、特异度及精确度。结果胰岛素+L-dopa联合激发试验激发峰值在非GHD组分别高于ARG、可乐定激发试验,在GHD组无差异显著性,胰岛素+L-dopa联合激发试验的特异度及精确度明显高于ARG和可乐定激发试验。结论胰岛素+L-dopa联合激发试验对儿童GHD的诊断价值优于ARG和可乐定激发试验,是一种适用于儿童的有效、简便、安全检测GH的方法。【关键词】生长激素缺乏症;生长激素激发试验;胰岛素;左旋多巴;精氨酸DiagnosticvalueofprovocativetestbyinsulincombinedwithlevodopaforgrowthhormonedeficiencyinchildrenCAIZhen-wei,LIUXiao-qiao,XIONGAn-xiou,WANG-Ming,ZHANGGuang-huan.Yichangcitycentralhospitaldepartmentofpediatricsgrowthcenter443000【Abstract】ObjectiveToevaluatediagnosticvalueofprovocativetestbyinsulincombinedwithlevodopa(L-dopa)forgrowthhormonedeficiency(GHD)duringchildhood.MethodAccordingtogrowthbibliographyandclinicalmanifestations,219childrenweredividedintotwogroups.GroupGHDcomprised119childrenwithappropriateauxotrophiccharacteristics,whiletheotherswereGroupNGHD(non-GHD).DetectedallchildrenbytheInsulin&L-dopajoint,arginine(ARG)andclonidineprovocationtest.AdoptedtheserumGHlevelsbeforethetestsandafterthetimeat30min,60min,90min,120minbyradioimmunoassayrespectively.AnalyzedtwosetsofexperimentsGHexcitationpeak,sensitivity,specificityandaccuracyatlast.ResultsInnon-GHDgroupthemeanpeakGHresponsetoinsulincombinedwithL-dopatestwasobviouslyhigherthanthattoarginine(ARG)testandclonidinetestatthesametimepoint;whileinGHDchild,thevalueshowednoapparentdifferencebetweenInsulin&L-dopajoint,arginine(ARG)andclonidineprovocationtestatthesametimepoint.ThespecificityandaccuracyofInsulin&L-dopajointprovocationtestwassignificantlyhigherthanthatARGtestandclonidinetest.Conclusions:Thediagnosticvalueofinsulin&L-dopatestisadvancedthanthatofARGtestandclonidinetest.Theprovocativetestusinginsulin&L-dopaisaconvenient,usefulandsafediagnosticmeansinchildren.【Keywords】Growthhormonedeficiency;Growthhormoneprovorativetest;insulin;L-dopa;arginine儿童的生长发育受到遗传、环境及营养因素影响[1],生长激素(GH)缺乏是引起儿童生长迟缓的最常见内分泌因素,在矮小儿童中大约占6%~10%,因此血清GH检测是临床对GHD的重要诊断依据,由于GH的分泌是脉冲式的,所以临床确诊GHD至少需要行两种GH激发试验[2],为探讨生长激素激发试验在矮小儿童中的诊断价值,本研究试采用胰岛素+左旋多巴(L-dopa)联合激发试验与精氨酸激发试验和可乐定激发试验检测GH的试验比较,评价其对儿童生长激素缺乏症的诊断价值。1资料与方法1.1一般资料2009年1月至2012年6月期间在我院儿科生长发育中心因身材矮小就诊且尚未接受任何治疗的儿童,所有入围儿童经初步检查排除甲状腺功能低下、小于胎龄儿、染色体异常、肝肾疾病、其他慢性器质性疾病及营养不良等,根据生长学资料、临床特征分为临床拟诊GHD组和非GHD组。生长学资料主要包括就诊时身高、最近至少6个月的身高生长速度、生长趋势。1.2分组标准GHD组:按骨龄的生长速度≤同年龄同性别正常均值第10百分位和(或)生长趋势显示衰减式生长,伴有GHD面容、小阴茎、异常围产史、中枢神经系统受损史等;非GHD组:近期6个月生长速度>同年龄同性别正常均值第10百分位且生长趋势呈非衰减式生长,生长资料显示既往有暂时性生长阻滞、患儿身高在靶身高范围内、有青春期发育延迟家族史。1.3入围病例的临床资料:GHD组:119例(男79例,女40例),中位年龄10.3岁,其中40例有GHD面容,20例有小阴茎,18例有异常围产史,3例行头颅MRI有脑部肿瘤;非GHD组:100例(男62例,女38例),中位年龄9.5岁,其中暂时性生长阻滞致矮小65例,家族靶身高矮小18例,有青春期发育延迟家族史17例。1.2方法1.2.1试验方法所有入围病例于试验第1天行精氨酸激发试验,第2天行可乐定激发试验,第3天行胰岛素+L-dopa联合激发试验,3次试验间隔时间均为24小时,均于生长发育中心凌晨8AM空腹(>2岁空腹8小时,<2岁空腹6小时)进行,试验全过程禁食。⑴、精氨酸激发试验:25%精氨酸0.5g/kg加生理盐水稀释至10%于30分钟内静脉滴入,于0min,静脉滴入后30,60,90,120min静脉采血查GH。⑵、可乐定激发试验:口服可乐定0.15μg/kg,服药前及服药后30,60,90,120min静脉采血查GH。⑶、胰岛素+L-dopa联合激发试验:常规胰岛素0.05-0.1u/kg加生理盐水5ml缓慢静脉注射,同时口服L-dopa10mg/kg,于0,30,60,90,120min静脉采血查GH,同时用微量血糖仪监测静脉血糖,血糖降至基础值50%以下或血糖低于2.8mmol/L为有效激发。1.2.2检测方法血清GH检测采用放射免疫分析法,仪器为拜耳magLami200型,检测试剂由深圳新产业生物医学工程有限公司提供,按试剂盒和仪器说明书操作,检测灵敏度0.01μg/L。1.3评价标准⑴、GH激发峰值,采用u检验分析;⑵、敏感度:临床拟诊GHD组病例中GH激发峰值<正常截断值的例数/临床拟诊GHD病例总数;⑶、特异度:临床拟诊非GHD组病例中GH激发峰值≥正常截断值的例数/临床拟诊非GHD组病例总数;GH激发峰值正常截断值按国际标准取10μg/L。2结果2.1胰岛素+L-dopa联合激发试验激发GH峰值在非GHD组(11.09±5.42)μg/L,在GHD组(4.10±4.76)μg/L,两者差别有意义(u=10.043>2.58,P<0.01)。2.2分别与精氨酸激发试验、可乐定激发试验比较,胰岛素+L-dopa联合激发试验激发GH峰值在非GHD组高于精氨酸激发试验(5.78±5.94)μg/L和可乐定激发试验的GH峰值(8.8±4.75)μg/L,两者差别均有意义(u=6.60>2.33,p<0.01和u=3.176>2.33,p<0.01);胰岛素+L-dopa联合激发试验激发GH峰值在GHD组与精氨酸激发试验(3.26±3.15)μg/L和可乐定激发试验的GH峰值(4.42±4.33)μg/L的差别无显著意义(u=1.607<1.64,p>0.05和u=0.543<1.64,p>0.05)。2.3诊断敏感度、特异度在GHD组,胰岛素+L-dopa联合激发试验的敏感度0.92(109/119),精氨酸激发试验敏感度0.92(110/119)、可乐定激发试验的敏感度0.94(111/119);在非GHD组,胰岛素+L-dopa联合激发试验的特异度0.53(53/100),精氨酸激发试验0.34(34/100)、可乐定激发试验的特异度0.33(33/100);胰岛素+L-dopa联合激发试验准确度0.79(162/219),精氨酸激发试验与可乐定激发试验的准确度均为0.66(144/219)。表1GH激发试验的敏感度、特异度比较组别激发试验敏感度特异度准确度GHD组胰岛素+L-dopa0.92(109/119)--精氨酸0.92(110/119)--可乐定0.94(111/119)--非GHD组胰岛素+L-dopa-0.53(53/100)精氨酸-0.34(34/100)可乐定-0.33(33/100)胰岛素+L-dopa--0.79(162/219)精氨酸--0.66(144/219)可乐定--0.66(144/219)3讨论影响小儿生长的原因众多,而且机制复杂,深入探讨不同类型矮小症的病因机制是提高矮小症临床诊疗水平的基础。研究表明,下丘脑、垂体及其胰岛素样生长因子(IGF)轴功能异常是矮小儿童的主要原因。根据GH、IGF检测结果可将生长障碍的病因分为4类:⒈GH、IGF均缺乏,肯定为GHD;⒉GH正常,IGF缺乏,属GH不敏感综合征;⒊GH缺乏但IGF正常,为可疑GHD;⒋GH和IGF皆正常,为特发性矮小症。人GH是由垂体前叶分泌的一种糖蛋白激素,他的主要作用是促进肝脏释放葡萄糖,促进脂肪分解与氧化,促进蛋白质合成,刺激颅骨、下颌骨增大及软骨肥大、骨骺软骨增生,进而促进生长。GH缺乏是引起儿童生长迟缓、身材矮小的常见内分泌因素,因此,检测血清GH水平是临床上诊断GHD的主要依据,但GH呈脉冲式分泌,昼夜波动大,一次随机检测基础状态下血清GH不足以反映垂体分泌GH功能,对诊断GHD无临床意义[3]。临床上多采用GH激发试验来检测血清GH水平。但任何一种刺激试验都有15%的假阳性率[4,5],因此,必须在两项刺激试验结果都不正常时,方能确诊GHD,本实验分别采用采用联合(胰岛素+L-dopa联合激发试验)或序贯激发(精氨酸激发试验和可乐定激发试验)。随着基因重组人生长激素(rhGH)的问世给GHD患者带来福音,其促进GHD患者身高生长的疗效显著,但其价格昂贵,因此在临床就需要一种诊断GHD准确性高的方法,但作为临床确诊GHD主要检测方法GH激发试验准确性受多种因素影响,如药物激发效能、配伍、性别、年龄、激素水平、代谢状况等。有学者认为,采用联合或序贯激发可优于单种药物激发,而且如果两种药物作用途经不同,作用效果更好[6,7]。精氨酸是通过介导与抑制生长激素抑制激素(GHIH)的分泌使GH释放增多;可乐定属兴奋α肾上腺素能受体,促进GHRH分泌,以促进GH的应答反应,使GH水平增高;胰岛素诱发急性低血糖是刺激GH分泌的强烈素,当血糖<2.8mmol/L或低于基础值一半以上时,可使GH明显升高;L-dopa是儿茶酚胺能神经递质,能刺激分泌GH释放激素(GHRH),使GH升高,是较强的口服激素药物,其重复性好,而且作用途经与胰岛素不同,两者联合使用可增强激发效能。本研究表明,在非GHD组,胰岛素+L-dopa激发试验激发峰值高于精氨酸激发试验和可乐定激发试验,而且对GHD诊断的特异度、准确度优于精氨酸激发试验和可乐定激发试验;在GHD组,胰岛素+L-dopa激发试验激发峰值并不比精氨酸激发试验和可乐定激发试验高,不会造成更多假阴性结果,此结果表明,无论在诊断GHD方面,还是早排除GHD方面,胰岛素+L-dopa激发试验的特异性、准确性都优于精氨酸激发试验和可乐定激发试验。本研究表明,胰岛素+L-dopa联合激发试验对儿童GHD诊断价值优于精氨酸激发试验联合可乐定激发试验,无严重不良反应,采血次数少,可增加患儿的依从性,并且住院时间短,住院费用少,是一种适用于儿童的有效、简便、安全检测GH的方法。参考文献[1]陈凤生.生长激素缺乏症的原因、分类和治疗[J].中国实用儿科杂志,1999,7(14):389-390[2]张文,宋向凤,王辉.人生长激素基因在小鼠体内的高表达[J].新乡医学院学报,2003,20(4):232-234[3]颜纯,王慕荻.小儿内分泌学[M].(第1版).北京:人民卫生出版社,2006,95-96[4]梁河涛,马玉华,谢为.81例矮小儿童生长激素的分析及临床意义[M].四川医学,2007,28(7):712-713[5]TanakaT.Globalsituationofgrowthhormonetreatmentingrowthhormone-deficientchildren[J].HormRes,1999,51(13):75-80(PMID:10592448)[6]GhigoE,BelloneJ,AimarettiG,etal.Reliabilityofprovocativeteststoassessgrowthhormonesecretorystatus.Studyin472norallygrowingchildren[J].JClinEndocrinolMetab,1996,81(9):3323-3327(PMID:8784091)[7]CarelCJ,TrescaJP,LetrailM,etal.Growthhormonetestingforthediagnosisofgroethhormonedeficiencyinchildhood:apopulatineregister-basedstudy[J].JClinEndocrinolMetab,1997,82(7):2117-2121(PMID:9215281)
蔡正维 主任医师 宜昌市中心人民医院 儿科5487人已读 - 精选 宜昌地区156例矮小儿童染色体核型分析
蔡正维刘孝桥付爱红潘芹(三峡大学第一临床医学院湖北省宜昌市中心人民医院,宜昌443003)摘 要:目的:分析矮小儿童的染色体异常。方法:对156例矮小儿童进行外周血染色体检查,采用常规外周血淋巴细胞培养,G显带,油镜下每例计数30个中期分裂相,分析5个核型,对异常核型增加核型分析数,进行核型分析。结果:156例受检者,共检出异常核型32例。占20.5%。其中常染色体异常3例,占1.9%,其中21三体综合征单纯型1例,表现为智力低下,先天性心脏病,典型愚形面容,身材矮小。另2例为21三体综合征嵌合型,表现为身材矮小外,其他表现不明显。其中性染色体异常29例,占18.6%。分别为性染色体数目异常18例,性染色体结构异常11例。结论:染色体异常是儿童身材矮小的一个重要原因,应引起临床医师的高度重视,特别是女童,应作为矮小诊断的常规检查。以免误诊漏诊。关键词:矮小儿童染色体异常核型分析ReportonBloodChromosomesKaryotypingResultin156casesofidiopathicshortstatureinYichangarea(Caizheng-wei,Liuxiao-qiao,Fuai-hong,PanqinTheFirstCollegeofClinicalMedicalScience,ChinaThreeGorgeUniversity,Yichang443003,China)Abstract:Objective:Toanalyzetheabnormalchromosomalkaryotypesfromperipheralbloodofidiopathicshortstature.Methods:Peripheralbloodchromosomeexaminationwasconductedin156undersizedchilgrenbyroutineperipheralbloodlymphocytesculture.SlideswereprocessedforG-bandingwithTrypsin-Giemsabystandardtechniques.Results:32frequenciesofchromosomeabnormalitiesweredetectedin156cases,therateofabnormalkaryotypeswas20.5%.Therewere3autosomalabnormalitiesand29sexchromosomeabnormalities.Conclusions:Theabnormalityofchromosomewasoneoftheimportantreasonsofidiopathicshortstature.Itisnecessarytoanalysechromosomeinidiopathicshortstature,especiallyingirls.Keywords:Chromosomekaryotypeanalysis,Abnormalchromosomekaryotypes,Idiopathicshortstature身材矮小是指与同地区同年龄同性别健康儿童比较,身高低于正常身高的2SD以上,或低于健康儿童生长曲线的第3个百分位[1]。身材矮小是儿科内分泌常见的症状,可由多种因素造成,染色体异常是其中一个重要原因。我们对2004年1月至2012年12月156例矮小儿童进行外周血染色体检查。现报告如下。1资料与方法1.1对象2004年1月至2012年12月在儿科生长发育门诊的156例矮小儿童,其中男32例,女124例。年龄范围14岁以下。1.2方法按我院细胞遗传室常规外周血淋巴细胞培养制作染色体标本,每例患者均在无菌操作下抽取静脉血2ml,肝素抗凝,取0.5ml接种于外周血淋巴细胞培养基(北京易世盛达公司生产)内,置CO培养箱37℃培养68~72h,10μg/ml秋水仙素50μl,作用3h后收获细胞制片,80℃烤片1h,胰酶法G显带。每例标本选取30个中期分裂相,分析5个核型,对异常核型增加核型分析数,进行核型分析。2结果156例受检者,共检出异常核型32例。占20.5%。其中常染色体异常3例,占1.9%,其中21三体综合征单纯型1例,表现为智力低下,先天性心脏病,典型愚形面容,身材矮小。另2例为21三体综合征嵌合型,表现为身材矮小外,其他表现不明显。其中性染色体异常29例,占18.6%。分别为性染色体数目异常18例,性染色体结构异常11例。29例性染色体异常核型及主要症状见表1。表1性染色体数目异常18例结构异常11例核型及主要临床表现核型例数主要表现45,XO8身材矮小45,XO/46,XX3身材矮小47,XXX/45,XO2身材矮小47,XXX/46,XX/45,XO1身材矮小47,XYY,21s+/45,XO,21s+1身材矮小、精神运动发育迟缓47,XXX1身材矮小47,XXY2身材矮小45,XO/46,X,iXq2身材矮小、男性乳房发育45,XO/46,X,iXp1身材矮小46,XO,+mar/45,XO1身材矮小46,XY女假2身材矮小、两性畸形46,XX男假5身材矮小、两性畸形3、讨论染色体数目异常和结构畸变是导致身材矮小的重要原因之一,在身材矮小的患儿中,常染色体核型异常最常见的为21三体综合征。21三体综合征分为单纯型、易位型、嵌合型。嵌合型临床表现比单纯型轻,一般21三体型细胞占9%以上才出现临床症状。嵌合型患者,也是随着三体型细胞数的增多而症状越重。本文在156例矮小儿童中检出常染色体异常3例,占1.9%,其中21三体综合征单纯型1例,表现为智力低下,先天性心脏病,典型愚形面容,身材矮小。另2例为21三体综合征嵌合型,表现为身材矮小外,其他表现不明显。在身材矮小的患儿中,性染色体核型异常最常见的为Turner综合征。Turner综合征又称先天性卵巢发育不全。患者表型为女性,智力大致正常,但常低于同年龄、同性别正常儿童水平。在存活女婴中发生率为1/2500~1/2000,其临床表现为身材矮小、性幼稚等症状[2]。Turner综合征的细胞遗传学十分复杂,除典型的45X0外,还报道过多种嵌合体和结构异常的变异型核型。45X0是Turner综合征的典型核型,其发生率约为55%。其他核型如45X0/46XX、45X0/47XXX等占45%。对于嵌合体核型,由于正常的合子细胞在某次有丝分裂中染色体发生不分离,形成异常的细胞,继续分裂后,将构成异常的细胞系,与正常细胞并存,形成嵌合体。由于遗传物质丢失量不同,Turner综合征患儿的临床表现亦不一致,即核型与表型之间存在依赖性。Turner综合征临床症状的轻重主要取决于正常与异常细胞所占比例,46XX占的比例越大,其临床异常表型越轻。另外,在青春期前,身材矮小可能是其唯一的表现。故对诊断为矮小的女童应注意同时检查染色体。Turner综合征的细胞遗传学复杂,除典型的45X外,还有嵌合和各种结构异常的核型,是女童矮小的重要原因。本组156例患儿中性染色体异常29例,其中Turner综合征19例,占65.51%;男或女假两性畸形7例,占24.13%.Turner综合征是性染色体异常中最常见的疾病,临床特征为:生长落后、性发育不良以及特殊的躯体特征身材矮小、蹼颈、肘外翻等[3]。5例男性假两性畸形,多见于睾丸女性化综合征,表现为女性体型,女性外生殖器,阴蒂肥大,睾丸常位于腹腔、腹股沟或大阴唇内,核型46,XY。有2例因腹股沟斜疝入院手术,术中行剖腹探查,发现盆腔内无卵巢、子宫及输卵管,阴道盲端。病检:性腺均为睾丸组织。2例女性假两性畸形,患儿女性内生殖器,有卵巢,外生殖器男性化,多伴尿道下裂,核型46,XX。此类患儿多为先天性肾上腺皮质增生症,属常染色体隐性遗传病,这种病人手术矫正并用肾上腺皮质激素类药物治疗可有月经[4]。矮小儿童的治疗主要是用重组人生长激素,而Turner综合征使用剂量较其他原因致矮小的偏大[5]。文献报道,5岁开始治疗,Turner综合征最终身高基本能达到正常水平。而一般患儿就诊普遍偏晚,到青春期性不发育来诊者居多,为早期得到诊断和治疗,对矮小女童常规染色体检查,以利于早期诊断早期治疗,避免错过最佳生长期。总之,染色体异常是儿童身材矮小的一个重要原因,应引起临床医师的高度重视,特别是女童,应作为矮小诊断的常规检查。以免误诊漏诊。参考文献[1]颜纯,王慕逖.小儿内分泌学[M].北京:人民卫生出版社,2006:104-130.[2]ElleuchM,MnifFM,KammounM,etal.Descriptiveanalysesofturnersyndrome:49casesinTunisia[J].AnnEndocrinol(Paris),2010,71(2):111-116.[3]王怡芳,樊启芳,张水林,等.新婚夫妇染色体筛查1214例调查分析J.中国优生与遗传杂志,2003,11(2):391[4]李桦,张小琼,等.儿童智力低下434例染色体异常核型分析M.中国优生与遗传杂志,2000,8(1):34-351[5]谢理玲,杨玉,杨利.Turner综合症的核型与临床表现[J].实用临床医学,2009,10(9):1-2.
蔡正维 主任医师 宜昌市中心人民医院 儿科3394人已读 - 精选 GnRHa激发试验与GnRH激发试验对性早熟的诊断价值的比较研究
宜昌市中心人民医院儿科生长发育门诊 蔡正维 刘孝桥 黄懿娟 王敏 熊安秀性早熟是儿科生长发育门诊常见疾病之一。就诊患儿以女童居多。传统的2小时促性腺激素释放激素(GnRH)激发试验是诊断中枢性性早熟(CPP)的金标准[1]。促性腺激素释放激素类似物(GnRHa)的生物活性是天然GnRH的数百倍,较天然GnRH具有更强的激发垂体促卵泡激素(FSH)及促黄体生成激素(LH)的合成和释放作用[12] [16],从而更强地激发24h性腺性激素的分泌。故GnRHa激发试验对于儿童性早熟鉴别诊断有很好的应用价值[2]。本文就 GnRHa激发试验和GnRH激发试验对于性早熟的诊断价值进行比较,并探讨临床应用GnRHa激发试验诊断性早熟的可行性。对象和方法一、对象选择我院儿科生长发育门诊在2009年5月至2011年12月因乳房发育提前(<8岁)而就诊的女性儿童87例,年龄5-9.5岁,骨龄5-11.5岁,初诊时均有乳房发育(TannerⅡ期54例,TannerⅢ期16例,TannerⅣ期7例), 乳房发育时间1周-2年,出现阴毛1例,有阴道分泌物9例,均无阴道出血,所有病例临床均排除肿瘤,罕见综合征及其他内分泌疾病,患儿均随访0.5-1.0年。二、方法1.将87例女孩随机分成两组,44例为GnRHa激发试验组,43例为GnRH激发试验组。2.GnRHa激发试验组,于就诊时行0,30和60分钟GnRHa激发试验,GnRHa激发试验方法是:于上午8-9时行皮下注射GnRHa(Decapeptyl,达必佳,辉凌(德国)制药公司)100ug/m,分别于注射后0,30和60分钟采血测定血清促卵泡激素(FSH)和促黄体生成激素(LH)浓度。如峰LH浓度>5.05IU/L和峰LH/FSH>0.44,则诊断CPP,反之则诊断PPP,如激发峰值以FSH升高为主,LH/FSH比值低下,结合临床可能是PT。3.GnRH激发试验组,于就诊时行0,30,60,90分钟GnRH激发试验,促性腺激素释放激素(GnRH)激发试验方法:于上午8-9时行静脉注射GnRH(戈那瑞林,上海丽珠东风制药厂)2.5ug/kg(最大剂量100ug),于注射的0,30,60和90分钟测定血清LH和卵泡刺激素(FSH)水平。如峰值LH>5.0IU/L和峰LH/FSH比值>0.6,则诊断CPP,反之则诊断PPP,如激发峰值以FSH升高为主,LH/FSH比值低下,结合临床可能是PT。4.均采用免疫化学发光法(MEIA)测定。5.统计学方法 χ检验阳性率差异性 病例总数 CPP PT PPPGnRHa 44 23 (22.3) 16 (16.7) 5(5.1)GnRH 43 21 (21.7) 17(16.3) 5(4.9)87 44 33 10P﹥0.05 无显著差异峰值时间差异性30分60分90分44(GnRHa)40(90.9%)4(9.1%)043(GnRH)26(60.5%)13(30.2%)4(9.3%) 病例总数 30分内峰值 30分后峰值GnRHa 44 40 (33.4)a 4(10.6)bGnRH 43 26 (32.6)c 17(10.4)d 87 (n) 66 21P〈0.01 有显著差异结果1.44例GnRHa激发试验组女孩中,峰值出现在30分钟者占90.9%,出现在60分钟者占9.1%,其中CPP23例,占52.3%,PT16例,占36.4%,PPP5例,占11.4%。2.43例GnRH激发试验组女孩中,峰值出现在30分钟者占60.5%,出现在60分钟者占30.2%,出现在90分钟者占9.3%,CPP21例,占48.8%,PT17例,占39.5%,PPP5例,占11.6%。3.两组比较,阳性率差异性P>0.05,差异无显著性,而峰值时间差异性P〈0.01 ,有显著差异。4.随访结果:诊断CPP者,乳房发育持续进行,生长速度加快,骨龄进展明显。诊断PT者,无生长速度加快,骨龄进展不明显,乳房结节在3至10个月完全消失。诊断PPP者,乳房结节均在6个月内完全消失。讨论随着环境和生活方式的改变,因乳房发育提前而就诊的女孩逐渐增多,乳房发育提前的常见病因包括真性性早熟(CPP),乳房早发育(PT),假性性早熟(PPP)。CPP是下丘脑-垂体-性腺轴(HPGA)功能提前发动所致的早熟,又称GnRH依赖性性早熟;PPP是除HPGA功能的发动外的异常性激素分泌所致的早熟(非GnRH依赖性性早熟) [6];单纯性乳房早发育(PT)是青春发育的一种变异类型,也有学者认为属不完全性早熟类型,并非由HPGA功能发动所致[6]。三者干预不同,因此鉴别尤为重要,一般临床上根据单次测量LH、FSH值及骨龄、卵巢、子宫的检查来判断真假性早熟较为困难,需做GnRH激发试验[4]。黄体生成素释放激素(LHRH)是下丘脑分泌的一种多肽激素,能刺激已发育成熟的垂体前叶分泌促性腺激素(LH、FSH)。传统的放射免疫法(RIA)测定基础血清FSH、LH和E2对性早熟性质没有诊断价值[7]。特别是病程较短(女孩乳房TannerⅡ期及部分Ⅲ期)、临床怀疑真性性早熟的女孩,由于尚未呈现典型的青春期特点,其临床早期诊断有困难。注射外源性LHRH后真性性早熟患儿因下丘脑-垂体-性腺轴已启动,注射后30分钟出现LH、FSH的高反应值,以LH升高为主;而假性性早熟因无下丘脑-垂体-性腺轴的启动,故无反应或反应较弱,而单纯性乳房早发育(PT)则以FSH升高为主[7]。故LHRH激发试验是诊断CPP的比较好的指标,也是CPP治疗后监测的重要手段。但LHRH激发试验需要测定0、30、60、90分钟的血标本[8],采血次数多,需要时间较长,而且LHRH(戈那瑞林)需要静脉注射,患儿依从性较差。促性腺激素释放激素类似物(GnRHa)是在天然的促性腺激素释放激素(GnRH)分子结构上进行修饰的一种肽类物质。GnRHa的生物活性是天然GnRH的数百倍,较天然GnRH具有更强的激发垂体FSH和LH的合成和释放作用[8] [12],从而更强地激发24小时性腺性激素的分泌。因此GnRHa激发试验对于儿童性早熟鉴别诊断和治疗监测中的应用价值值得探讨。本文结果显示,两组乳房提前发育的女孩中,GnRHa激发试验组44例,诊断CPP23例,占52.3%,PT16例,占36.4%,PPP5例,占11.4%。GnRH激发试验组43例,CPP21例占48.8%PT17例占39.5%PPP5例占11.6%。两组比较,P>0.05,差异无显著性。结合随访结果看,GnRHa激发试验与GnRH激发试验对性早熟性质均具有鉴别诊断意义。44例GnRHa激发试验组女孩中,峰值出现在30分钟者占90.9%,出现在60分钟者占9.1%。43例GnRH激发试验组女孩中,峰值出现在30分钟者占60.5%,出现在60分钟者30.2%,出现在90分钟者占9.3%,峰值时间差异性P〈0.01 有显著差异。与传统的GnRH激发试验相比,GnRHa激发试验采血次数减少,并较大程度地减少了检查费用, GnRHa(达必佳)采用皮下注射,较LHRH(戈那瑞林)静脉注射痛苦小,患儿依从性好。而且采用免疫化学发光法(MEIA)较传统的放射免疫法(RIA)灵敏度更高[9]。具有较高的诊断真性性早熟的灵敏度和特异度,有助于早期诊断,因而具有较大的实用价值。参考文献1. Wacharasindhu S,Serivuthana S,A roonparkmongkol S.et al.A cost-benefit of GnRH stimulation test in diagnosis of central precocious puberty(CPP)[J].J Med Assoc thai,2000 83(9):1105-11112. 马华梅,杜敏联等.GnRHa激发试验对性早熟的诊断价值探讨. 中国实用儿科杂志,2002,17(5):290-2933. Prescovitz, OH, Hench HD, Barnes KM, et al. Premature thelarche and central precocious puberty: the relationship between clinical presentation and the gonadotropin response to luteinizing hormone releaseing hormone. J Clin Endcorinol Metab, 1988,61(3):4744. Noely EK, Hintz RL, Wilson DM, et al. Normal ranges for immunochemi-luminometric gonadotropin assays, J Pediatr, 1995,127(1):405. Oerter KE, Uriarte MM, Rose SR, et al. Gonadotropin secretory dynamics during puberty in normal girls and boys, J Clin Endcorinol Metab, 1990,71(5):12516. Neely EK, Wilson DM, Lee PA, et al. Spontaneous serum gonadotropin concentrations in the evaluntion of precocious puberty, J Pediatr, 1995,127(1):477. Oerter KE, Uriarte MM, Rose SR, et al. Gonadotropin secretory dynamics during puberty in normal girls and boys, J Clin Endcorinol Metab, 1990,71:1251-12588. Cutler Jr GB. Precocious Puberty In: Hurst JW, ed. Medicine for the practicing physician. Boston Butterworth, 1988,526-5309. Carallo A, Zhou X. LHRH test in the assessment of puberty in normal children. Horm Res, 1994, 41:4110-411510. Garibaldi LR, Picco P, Magies S, et al. Serum luteinizing hormone concentrations, as measured by a sensitive immunometric assay in children with normal, precocious or delayed pubertal development. J Clin Endcorinol Metab, 1991,72:888-89811. Sulerno M, Di Maio S, Gasparini N, et al. Central precocious puberty: a single blood sample after gonadotropin releasing hormone agonist administration in mornitoring treatment. Morm Res, 1998,50:205-21112. Palmert MR, Malin HV, Boepple PA. Unsustained or slowly progressive puberty in young girls: initial presentation and cong time follow up of 20 untreated patient. J Clin Endcorinol Metab, 1999,84:415-42313. Prescovitz OH, Hench HD, Barnes KM, et al. Premature thelarche and central precocious puberty: the relationship between clinical presentation and the gonadotropin response to luteinizing hormone releaseing hormone. J Clin Endcorinol Metab, 1988,61(3):474-47914. Cavallo A, Richards GE, Buseys, et al. A simplified gonadotrophin releasing hormone test for precocious puberty. Clin Endcorinol, 1995, 42:641-64615. Ghai K, Rosenfield RL. Maturation of the normal pituitary testicular axis, as assessed by gonadotrophin releasing hormone agonist challenge. J Clin Endcorinol Metab, 1994,78:1336-134016. 15 Ibanez L, Potan N, Zampoui M, et al. Use of leuprolide acetate response patterns in the early diagnosis of pubertal disorders comparison hormonal carcinogenesis gonadotropin-releasing hormone test, J Clin Endcorinol Metab, 1994,78(1):30
蔡正维 主任医师 宜昌市中心人民医院 儿科1.5万人已读 - 精选 宜昌市中心人民医院成功举办省级继续教育项目“儿童生长发育相关疾病新进展学习班”“
11月3日,由市中心人民医院儿科主办省级继续医学教育项目“儿童生长发育相关疾病新进展学习班”在市中心医院学术报告厅成功举办。 随着小儿内分泌专业的蓬勃发展,儿童生长发育领域的理论不断得到更新,诊断和治疗方法不断得到提高。为了推广新的理论和治疗方法,不断推动宜昌市小儿内分泌专业特别是儿童生长发育领域的发展,医院儿科特举办了此次学习班。 学习班邀请了华中科技大学同济医学院附属同济医院罗小平教授,武汉市儿童医院姚辉教授等多位小儿内分泌专业的专家到场授课。罗小平教授,是主任医师,医学博士,博士生导师。现任华中科技大学同济医学院遗传代谢病诊断中心主任,同济医院儿科学系主任,遗传代谢内分泌病研究室主任。是湖北省儿科学会主任委员,全国儿科内分泌遗传代谢病学组组长;而且是加拿大多伦多大学医学院儿科学系兼职教授;亚太儿童内分泌学会主席;姚辉教授,是主任医师,医学博士。武汉儿童医院内分泌科主任,内分泌专业学科带头人,院中心实验室副主任,曾先后赴德国慕尼黑儿童中心及美国Nationwide儿童医院进修学习。两位教授均是儿科内分泌特别是儿童生长发育领域方面国内知名的专家。学习班由儿科主任王敏教授主持,纪委书记刘红斌同志致开幕词。参加这次学习班的有来自全省特别是来自全市各个县市医院、妇幼保健院的儿科同仁。 学习班讲授了“矮身材诊断程序及生长激素应用”;“性早熟”;“甲状腺功能低下与儿童矮小”;“生长激素的在生长发育相关疾病的应用”等生长发育相关疾病临床的新进展,吸引了我市多家医疗单位近200人参会,参会人员与专家进行了热烈的讨论,会后大家纷纷表示获益匪浅。 本次学习班最大的特点是务实,它向市县等兄弟单位介绍了我院儿科跨越式发展的经验,推动了我市儿科持续、健康、快速发展,更为广大的儿童带来了福音。
蔡正维 主任医师 宜昌市中心人民医院 儿科3775人已读 - 精选 孩子个矮怎么办 请听医生对您说
孩子的身高可能关系到孩子的升学、就业、成家,是每一位家长关心的,也是我们儿童保健医生关注的。一个人的生长是从母亲宫内的胎儿发育开始,经过婴儿期、幼儿期、学龄前期、学龄期的16-18年生长,达到最终身高,而每个阶段各方面的原因导致的生长问题,都会损害最终身高,使个子较矮。人的生长发育有两个高峰,一是婴儿期,另一个是青春期。在青春期创造各种有利条件,无疑能促进生长潜力的发挥。其中充分的营养、合理的体育运动,充足的睡眠以及保持愉快的心情是促进生长的四大要素。充足的营养 每天要摄取足够的热量和各种营养素,包括蛋白质,脂肪、碳水化合物,膳食纤维、维生素、无机盐和水分。这些营养素存在于粮食、蛋类、肉类、奶类、蔬菜、水果等食物中。在生长突增时期,每天钙的摄入量应达到1000——1200毫克。奶制品水产品自制的含钙量较多,并且吸收利用程度较好,是补充钙的理想食品。体育活动 在保证营养供给充足的前提下,体育活动是促进身体发育和增加体质最有效的方法,体育锻炼能促进身体的新陈代谢,增强食欲,促进骨骼生长。充足的睡眠 充足的睡眠也是促进生长的一个重要因素,因为生长激素主要是在夜间深睡眠时分泌,青少年应保证每天有9-10个小时的睡眠。愉快的心情 好心情有利于生长激素的分泌以促进生长。小强是一个17岁的高一男学生,可身高只有138厘米。从出生至两岁小强生长基本正常,两岁以后生长逐渐减慢,与同龄孩子拉开距离,家长抱着侥幸的心理,认为“孩子可能晚生长”。上小学时,小强明显矮于其他同学。家长着急了,听说什么促长药,就买给孩子吃,或有什么助长器之类,就给孩子用上,花了不少钱,可是不见孩子长高。当孩子进入青春期,才来医院儿科就诊,经过检查,结合病史,诊断为生长激素缺乏症。用生长激素治疗一年长了13厘米。可是他的激素生长时间已不够了,最终身高是不理想的。宜昌中心医院儿科门诊中遇到的另一位男孩小明,同样是生长激素缺乏症,2岁开始减慢,4岁时与同龄孩子有一定的差距,父母很重视孩子的生长发育问题,及时带孩子上医院检查,通过医生的治疗,现已17岁身高168厘米,达到正常。因此,在孩子的生长发育中,家长应注意以下几点:1、孩子出生时是否正常,有否宫内发育迟缓,宫内发育迟缓的孩子有85%左右在12个月内能追赶上正常孩子的生长。如有异常,应及时就医,尽早治疗。2、孩子的正常的身高增长为:出生第一年增长25厘米,出生第二年增长10-12厘米,出生第三年至青春期前每年增值4-7厘米(注意每年身高增长最低限为厘米)如果孩子生长速度达不到正常的生长速度,应尽早做进一步检查。3、孩子的身高是否明显矮于同龄的孩子。4、注意孩子的第二性征的出现(如女孩乳房的增大,阴毛出现,男孩睾丸增大,阴毛出现等),警惕性早熟。如果女孩第二性征出现早于8岁,男孩早于9岁为异常,要进一步检查治疗。总之,家长应关心孩子每个时期的生长发育情况,如有疑问应尽早检查,以免造成终身遗憾。
蔡正维 主任医师 宜昌市中心人民医院 儿科4085人已读 - 精选 0-18岁儿童青少年、身高体重百分位数值表
孩子矮小,及早干预作为妈妈,你可知道孩子的身高是否在正常范围值内?可知道宝宝从出生后到青春期,每年应该长多少才算正常?生活中,我们又该怎样照顾孩子,才能让他健康成长呢?人体的最终身高和遗传、环境、营养、运动、睡眠、社会心理因素分不开,但如果你的孩子经过一个暑假,仍旧因为个头矮小而坐在班级的前三排,并且每年的生长速率低于5厘米,与同龄孩子的差距逐渐拉大时,你就要多加留意了,及早带孩子到儿科内分泌专科咨询检查。 注意儿童生长缓慢的信号儿童生长发育是有规律的,在青春期生长速度最快。到了青春期后,骨骼发育成熟,骨骺线闭合,身高就不再生长了,再用任何方法也无法使孩子继续长高。由于错过了给孩子治疗的最佳时机,很多家长只能遗憾终身。这就要求家长密切关注孩子的生长状况,及时发现孩子生长缓慢的信号。●儿童的生长速度3岁前小于7厘米/年●3岁到青春期小于5厘米/年●青春期小于6厘米/年实际上,随着医学的发展,儿童矮小症是可以治疗的。通过生长激素的替代治疗,很多矮小症患儿可以出现快速追赶式生长,达到比较理想的身高。
蔡正维 主任医师 宜昌市中心人民医院 儿科4万人已读 - 精选 宜昌市中心人民医院引进最先进的“化学发光法”检测生长激素
宜昌市中心人民医院引进最先进的“化学发光法”检测生长激素一年一度的暑期即将到来,暑期是儿童生长发育的黄金时期,也是身材矮小儿童就诊与治疗的高峰时期。为了让孩子更安全、准确、快捷的就诊与治疗。宜昌市中心医院儿科引进最先进的“化学发光法”仪器来检测生长激素,为广大身材矮小儿童带来福音。借此机会,记者采访了宜昌市中心人民医院儿童生长发育专家蔡正维主任。记者:什么是儿童生长激素缺乏症?“化学发光法的优点是什么?蔡主任:儿童生长激素缺乏症(growthhormonedeficiency,GHD)是由于神经垂体生长激素(GH)分泌不足所致的身材矮小,是导致儿童矮身材的重要原因。除生长激素缺乏症之外,还有性早熟导致的身材矮小,还有部分由于宫内发育迟缓或染色体异常等引起的。生长激素的检测方法有放射免疫法、酶联免疫法、免疫荧光法、化学发光法等,其中化学发光法具有良好的灵敏度和重复性、自动化程度高、无放射污染等诸多优点。生长激素激发试验能够快速、准确的诊断儿童生长激素缺乏症。宜昌市中心人民医院儿科早在2004年就独家开展生长激素激发试验,是宜昌乃至渝东鄂西最早开展这项业务的医院。这次“化学发光法”检测生长激素仪器的引进,再次让我们中心医院生长发育诊疗工作走在全市前列。记者:如何确认孩子身高是否存在问题?蔡主任:判断一个儿童的身高是否正常,是将其身高与同种族、同年龄、同性别的正常儿童的标准身高进行比较,这一标准身高是从大数量有代表性的健康儿童的体格测量中计算出来,可用标准差法或百分位法来表示。身高低于同龄同性别健康儿童的平均值减2个标准差或位于第三百分位以下者属于身材矮小。一般来说婴幼儿期(3岁以下)生长速度小于7厘米/年,儿童期(3岁-青春期)生长速度小于4-5厘米/年,青春期生长速度5.5-6.5厘米/年,即为生长发育迟缓。矮小儿童常有自卑心理,影响儿童身心健康及智力发育,缺乏与人沟通或主动参与社会活动的勇气,减少事业上成功的机会,未来就业范围也受到限制。因此身材矮小者应及时去医院进行进一步的诊断和治疗。记者:何时为治疗矮小的最佳时机?蔡主任:孩子矮小应早发现、早诊断、早治疗。年龄越小,骨骺的软骨层增生及分化越活跃,孩子生长的潜力及空间越大,对药物越敏感,生长效果越好,治疗所需费用越低。切不可等到发育后期如15-18岁,此时骨骺接近闭合,生长潜力很小,已不再可能达到理想身高,发现矮小也不要乱投医乱用药,更不要抱着等孩子晚长的幻想,以免骨骺闭合,失去长高的机会。记者:导致矮小的病因有哪些?发现孩子矮小怎么办?蔡主任:一种是生长激素缺乏性矮小,主要表现为胎儿期生长近乎正常,但在出生后生长减缓。儿童身高的增长自幼年期直至青春期均明显地落后于同年龄、同性别的正常健康儿童;一种是特发性身材矮小,是儿童期导致身材矮小的最常见原因,它是不伴有潜在病理状态的身材矮小;一种是小于胎龄儿,指出生体重和(或)身长低于同胎龄正常参考值两个标准差的新生儿。这种病症的发生率在人类胎儿中占有3%~10%,中国是7.5%。还有性早熟,先天性卵巢发育不全综合征等。我在每周五上午的专家门诊中看过的矮小患儿中,通过各种检查都能够发现矮小的病因,并有很多矮小患儿得到了治疗,取得了明显的效果。所以,家长们发现孩子身材矮小应及时到正规医院的儿科内分泌门诊就诊,可做各种检查以发现孩子矮小的原因,并根据不同的原因用不同的方法治疗。做到早发现,早诊断,早治疗,尽早干预效果好。只要及时就诊,多数矮小儿童都能得到有效的治疗。如果错过治疗时机(骨骺闭合),这些孩子将终生与“矮小”为伴。
蔡正维 主任医师 宜昌市中心人民医院 儿科4506人已读





